論文解説-3
Biochem Biophys. Res. Commun. 2021 In press.
G-patch domain-containing protein 4 localizes to both the nucleoli and Cajal bodies and regulates cell growth and nucleolar structure
解説1と2の論文で行ったプロテオミクス解析において同定された新規の核小体因子G-patch domain containing protein 4(GPATCH4、G4)というタンパク質の機能解析を行いました。G4はG-patchドメインと呼ばれるRNA結合因子など、RNA代謝に関わる因子に見られる領域を持つ因子です。一部のタンパク質が有するG-patchドメインはRNAやDNAに結合する活性を持つようですが、G4のG-patchドメインは機能的な役割はわかりません。本論文では、G4が遺伝子として同定はされていたものの、その局在や機能が不明だったため、G4の局在とリボソーム合成や核小体形成における役割を明らかにすることを目的として研究を行いました。G4はNPM1やNCLの複合体の構成因子として同定されたことから、核小体因子であることが想定されていましたが、実際、G4が核小体因子であることを証明しました。核小体のGCやDFCに主に局在するようです。また、FibrillarinやDKC1といったsnoRNPの構成因子と同様にCajal bodyと呼ばれるsnRNPやsnoRNP形成の場と考えられる核内構造体にも局在することがわかりました。G4ノックダウン細胞ではコントロール細胞に比べて細胞増殖が抑制され、FCやDFCといった核小体の中心領域の構造変化が観察されました。本論文では、G4が核小体やCajal bodyでどんな働きをしているのかを明らかにするには至りませんでしたが、核小体構造形成においても重要な役割を担っていることが想定されます。がん細胞でも発現亢進がみられることから、細胞のがん化ともかかわる可能性があります。
論文解説-2
BBA Molecular Cell Research 2021 Jan;1868(1):118879. doi: 10.1016/j.bbamcr.2020.118879.
The interaction between nucleophosmin/NPM1 and the large ribosomal subunit precursors contribute to maintaining the nucleolar structure
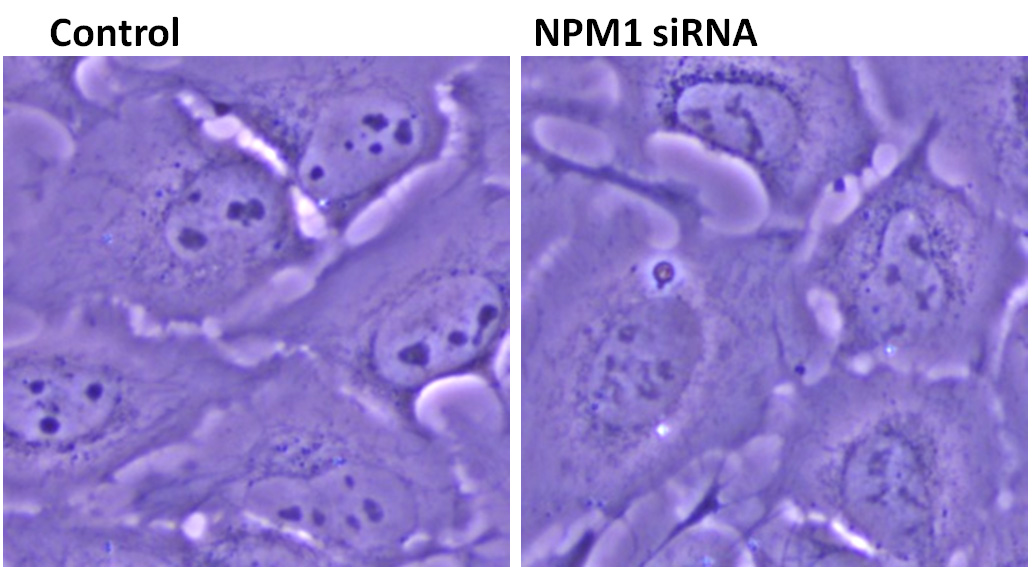
この実験はNPM1ノックダウン細胞の光学顕微鏡観察からスタートしました。NPM1をノックダウンすると、核小体の’黒さ’が減って、形も変になっています。なぜ?という疑問から、NPM1はリボソームの大サブユニット前駆体を核小体にとどめ、前駆体の成熟に関わると同時に、前駆体を核小体にとどめることで核小体のサイズを維持していることがわかりました。核小体のサイズは、増殖細胞の指標となっており、がんの病理診断の指標としても利用されます。多くの固形がんでNPM1の過剰発現がみられており、核小体の大きさを制御する重要な因子としてNPM1が重要であると考えられます。NPM1は液-液相分離を起こすことも報告されており、核小体の大きさとNPM1の関係に関しては引き続き研究を進めています。
論文解説-1
Journal of Biochemistry 2021 Feb 6;169(1):87-100. doi: 10.1093/jb/mvaa095.
RNA-recognition motifs and glycine and arginine-rich region cooperatively regulate the nucleolar localization of nucleolin
Nucleolin(NCL)は核小体に局在するリン酸化タンパク質で、がん細胞など増殖細胞で高発現している。NCLの過剰発現は、がんの悪性化と関わることが示唆されている。NCLはrRNAの転写を促進することで、細胞増殖を正に制御する。NCLのN末端にはヒストンH1様の領域、酸性アミノ酸に富む領域など特定の構造は取らないものの、ヒストンシャペロンあるいはクロマチン結合タンパク質として働くと考えられる領域を持つ。一方、C末端側はRNA recognition motif(RRM)と呼ばれるRNA結合領域を4つと、グリシン、アルギニンに富むGAR領域を持ち、直接RNAあるいはDNAに結合する。NCLは主に核小体に局在するが、核小体局在に影響を与える領域はよくわかっていない。NCLの核小体局在は上述の通りリボソーム合成に重要であることから、本研究ではNCLの核小体局在に影響を与える領域の同定を試みた。実験には、4つのRRMに点変異を導入し、機能不全とした変異体やGAR領域を欠損した変異体を用いた。結果としては、GAR領域とRRM4が、NCLの核小体局在に重要であることが明らかになった。また、試験管内の核酸結合活性の検討から、4つのRRMは標的の配列に依存しての使い分けられていることが示唆された。筑波大時代からの継続のテーマで、北里大薬学部生命創薬の学部4年生で配属された吉村くんが地道にFRAPの解析をやり直してきれいなデータとなりました。研究補助の茂木さんの実験が結果が掲載号の表紙に採用されました。