

当研究室では、主にオピオイド受容体に注目し、受容体選択的な化合物の創出に取り組んでいます。
旧Backgroundへはこちら
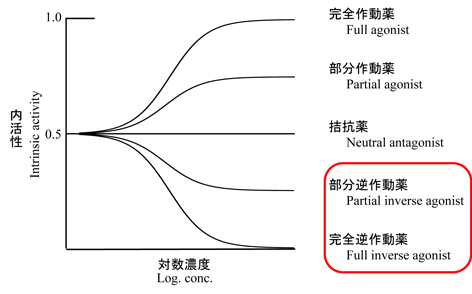
当研究室ではこれまでにδオピオイド受容体 (DOR) 拮抗薬であるNaltrindole (NTI)の構造活性相関研究においてDOR 逆作動薬を見出している1) 。一般に作動薬とは受容体に結合し正の活性を示す化合物であるが、逆作動薬は受容体に結合して負の活性を示す。(より正確に言えば、逆作動薬は化合物の有無に関係なく受容体が示す活性 (構成的活性と呼ばれる) を抑制する化合物である。この為、負の活性を示すように見える。)
オピオイド受容体に限らず逆作動薬の生理的意義には不明な点が多い。我々は現在より高活性なDOR逆作動薬の創出を目指すと共に生体内での作用を検討している2), 3) 。
1) Bioorg. Med. Chem. Lett., 2015, 25, 2927-2930.
2) ACS Chem. Neurosci., 2019, 10, 2237-2242.
3) ACS Chem. Neurosci., 2019, 10, 3939-3945.
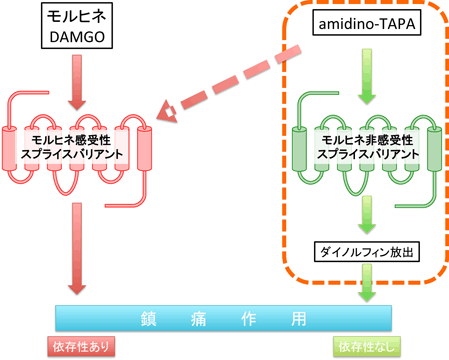
モルヒネなどの医療用麻薬が主に作用するオピオイドμ受容体には、異なる塩基配列を有する数十種類の受容体 (スプライスバリアント, SV)が存在することが知られている1)。このSVはモルヒネやμ受容体選択的ペプチド性作動薬であるDAMGOが作用するモルヒネ感受性SV(赤)と作用しないモルヒネ非感受性SV(緑)に大別することが出来る。モルヒネ非感受性SVを介した鎮痛効果はモルヒネ感受性SVと異なり、内因性オピオイドκ受容体作動性ペプチドであるダイノルフィン等の放出を介して鎮痛効果を示すため、非疼痛時においても薬物依存が形成されにくいと考えられる。
実際、モルヒネ感受性SVおよびモルヒネ非感受性SVに作用することが知られているオピオイドペプチドであるamidino-TAPAは鎮痛効果を示し2)、非疼痛下においても薬物依存を形成しないことが報告されている3)。このamidino-TAPAの構造的特徴を考慮し、モルヒネ非感受性SV選択的作動薬の創出を目指している。
1) Neuropharmacology, 2014, 76, 198-203.
2) a) Eur. J. Pharmacol., 2007, 560, 150-159., b) Eur. J. Pharmacol., 2011, 651, 66-72., c) Eur. J. Pharmacol., 2013, 711, 80-86.
3) Psychopharmacology, 2010, 212, 215-225.
4) ペインクリニック, 2017, 38, S196
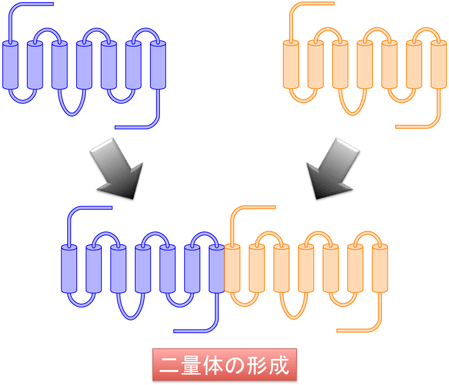
オピオイド受容体を含むG-タンパク質共役受容体 (GPCR) が同一(ホモ)または異なる(ヘテロ)受容体同士で二量化することが報告されている1)。GPCRの二量化は細胞レベルでだけではなく、げっ歯類2)やヒト3)の体内でも形成が認められており、新たな創薬ターゲットとして期待されている。
我々はオピオイド受容体が形成する二量化受容体選択的な化合物の創出を目指している。
1) Pharmacol. Rev., 2005, 57, 289-298.
2) (a) Sci. Signal., 2010, 3, ra54., (b) Br. J. Pharmacol., 2015, 172, 2507-2518.
3) Nature Med., 2001, 7, 1003-1009.
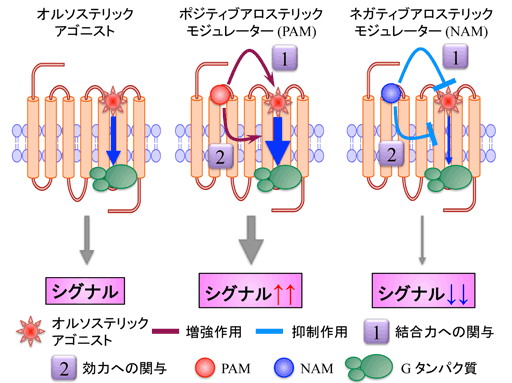
薬が作用する受容体の結合部位には、内因性のペプチド等が結合するオルソステリック部位とそれ以外のアロステリック部位が存在する。アロステリック部位に結合する化合物のうち、オルソステリックアゴニストの効果を増強するのはポジティブアロステリックモジュレーター (positive allosteric modulator, PAM)、逆にオルソステリックリガンドの効果を減弱するものはネガティブアロステリックモジュレーター (negative allosteric modulator, NAM)と呼ばれる。アロステリックモジュレーターは、オルソステリックリガンドよりも受容体選択性が出やすいと考えられており、副作用低減に繋がる創薬手法として注目されている1) 。
現在、各オピオイド受容体に対するアロステリックモジュレーターの創出を目指し、研究を行っている2) 。
1) Br. J. Pharmacol., 2015, 172, 277-286.
2) J. Pharmacol. Sci., 2018, 137, 67-75.

有機光化学反応は、従来の熱反応では合成が難しい医薬品の分子骨格を短工程で合成できる可能性がある。また熱反応と比較して多くの試薬を用いる必要がなく、グリーンな合成法となることがある。このため、海外のある製薬会社は光反応を用いる高効率的な医薬品プロセス合成を開始している。
我々も、第三級アミンの炭素−水素結合を活性化しエノンに対する不斉共役付加をエナンチオ選択的に進行させることができるキラル光触媒の創製等の研究を行っている。
Org. Biomol. Chem., 2015, 13, 8919-8924.
Heterocycles, 2018, 97, 591-603.
RSC Adv., 2020, 4, 388-392.
ChemPhotoChem, 2020, 4, 388-392.
Chem. Eur. J., 2021, 27, 5171-5179.